Dette går fram av Rabindra Khadkas doktorgradsarbeid i ingeniørvitenskap.
I dag må mange gjennom dyre hjerneskanninger eller ta prøver av ryggmargsvæske, for å utrede Alzheimer. Det kan være belastende og ikke alltid så lett å få gjort.
Hjernetesten EEG finnes derimot allerede på mange sykehus og klinikker, det er rimelig og gjør ikke vondt. Hvis vi kan lese tidlige sykdomstegn i EEG, kan flere få utredning tidligere.
– Målet vårt var å oppdage tidlig demens, slik at vi kan hjelpe disse menneskene, understreker Rabindra Khadka.
Slik fungerer det
- EEG fanger opp hjernens aktivitet. KI‑modellen lærer å kjenne igjen mønstre som henger sammen med Alzheimer.
- Når EEG‑data kombineres med enkel informasjon om personen, for eksempel alder eller resultater fra kognitive tester og annen klinisk informasjon, blir treffsikkerheten bedre.
- KI‑modellen trenes først på store mengder hjernesignaler for å bli god til å oppdage mønstre, og finjusteres deretter på mindre datasett der forskerne vet mer om deltakerne.
- I tillegg ser forskeren på korte, gjentakende mønstre i hjernesignalene. Disse kan gi enkle forklaringer som hjelper fagfolk å forstå hva modellen vektlegger.
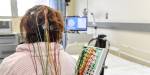
– Med elektroder på hodet i stedet for nåler får vi et vindu inn i hjernen, og ser hvordan den fungerer, forklarer Khadka.
Enklere, raskere og rimeligere
Dette er første gang noen har vist at EEG, sammen med demografisk og klinisk informasjon, kan anslå nivået av en Alzheimer-relatert blodmarkør, som kalles p-tau217.
Et skreddersydd KI‑rammeverk er utviklet for å fange hvordan hjerneaktiviteten utvikler seg over tid, samtidig som det forklarer hvordan det kommer fram til sine vurderinger.
Modellen er gjort lettere og raskere, slik at analysen i prinsippet kan kjøres på enklere utstyr nær pasienten.
– Så langt jeg vet, er dette første gang noen har forsøkt å forutsi p‑tau217 ut fra EEG. Resultatene er foreløpige, men svært lovende, sier Khadka.
Mindre belastning og bedre tilgang
– I praksis slipper pasienten en smertefull prosess med blodprøver eller tapping av spinalvæske. Hvis vi kan anslå nivået innenfor en viss feilmargin, er det et stort skritt framover.
Elektroder på hodet i stedet for nåler og dyre skanninger kan redusere belastningen for pasientene. EEG er også utbredt, og kan brukes flere steder i helsetjenesten.
– EEG er rimelig, bærbart og kan brukes ved mange klinikker og mindre sykehus, også i land med færre ressurser, sier Khadka.
– Med denne typen system får legene en ekstra assistent som gir tilbakemeldinger basert på en biomarkør, uten en lang og kostbar utredning.

Målet til Rabindra Khada er tidligere og mindre belastende demensutredning. Foto: Olav-Johan Øye
Mer forskning må til først
Resultatene må bekreftes i større og mer varierte pasientgrupper før metoden kan tas i bruk.
Det trengs også mer standardisering. EEG‑målinger kan variere fra sted til sted, og kvaliteten kan være ulik.
Neste steg er å vise hvor pålitelig modellens anslag er, og legge til rette for at sykehus kan samarbeide om å forbedre den uten å dele sensitive pasientdata.
– En stor begrensning i dag er mengden data. Modellen ble trent og evaluert på et begrenset antall datasett, og inkluderte få tilfeller med alvorlig demens. Metoden må testes bredere, og vi må vise hvor pålitelige anslagene er, sier Khadka.
– Hvis sykehusene samler inn mer data og vi fortsetter utviklingen, kan jeg se for meg at en robust standardmodell er klar innen fem år.
Personvern og forklarbarhet
Selv om data i dette prosjektet ble behandlet i sikre skytjenester, peker Khadka på løsninger som kan beskytte personvernet enda bedre.
– I framtiden kan data lagres lokalt på sykehus. Modellen kan også sendes sykehuset, trenes der, og tas tilbake uten å dele rådata.
– Noen klinikere er skeptiske til «svarte bokser» der det ikke er tydelig hvordan modellene kommer fram til resultatene. Derfor jobber vi for mer åpenhet og forklaringer i modellene.
Om doktorgraden
Rabindra Khadka har tatt doktorgrad ved OsloMet, Institutt for informasjonsteknologi, Fakultet for teknologi, kunst og design. Han har utviklet metoder som bruker EEG sammen med enkel personinformasjon for å anslå Alzheimer‑relaterte blodmarkører. Arbeidet vektlegger forklaringer som fagfolk kan forstå, og løsninger som kan fungere i praksis.